Ендоскопічне УЗД: що це таке і коли його слід використовувати?
Ендоскопічне ультразвукове дослідження (EUS) стає все більш доступним діагностичним і терапевтичним інструментом, який використовується у всьому світі. Він має широке застосування не тільки на органах шлунково-кишкового тракту, а і в середостінні, причому його поточне основне застосування полягає в визначенні стадії злоякісних новоутворень просвіту та оцінці уражень підшлункової залози та субепітелію. Поява лінійної ЕУЗД відкрила нові терапевтичні шляхи: аспірація тонкою голкою, трукат-біопсія, блокада целіакії та трансмуральне дренування псевдокісти. Майбутні розробки включають локалізовану брахітерапію/хіміотерапію та алкогольну абляцію неоперабельних злоякісних пухлин підшлункової залози та ендоскопічну хірургію під контролем ЕНДО УЗД.
Ендоскопічне ультразвукове дослідження (ЕУЗД) було розроблено в 1980-х роках, але в той час ще рідко використовувалося. Десятиліттям пізніше, коли з’явилися терапевтичні УЗД з використанням лінійних ехо-ендоскопів, зокрема можливість брати зразки лімфатичних вузлів і підозрюваних злоякісних новоутворень за допомогою аспірації тонкою голкою (FNA), призвели до її більшого поширення, хоча надання послуг все ще залишається централізованим у більшості регіонів. В цей час визначення стадії раку стравоходу та стравохідно-шлункового з’єднання у пацієнтів, потенційно придатних для лікувальної хірургії, залишається найпоширенішим показанням до ЕУЗД.
Що таке ендоскопічне УЗД?
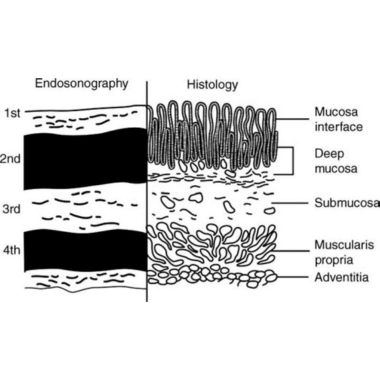
Ендоскопічне ультразвукове дослідження поєднує в собі два способи ендоскопічної візуалізації з високочастотним ультразвуком, щоб забезпечити зображення стінки органів шлунково-кишкового тракту (ШКТ) і за його межами в органах і судинах, розташованих поблизу. Визначити кожен із п’яти шарів стінки шлунково-кишкового тракту, що відповідає його гістологічному аналогу, а також виявити локалізовані лімфатичні вузли є основою для більшості процедур УЗД (мал. 1).
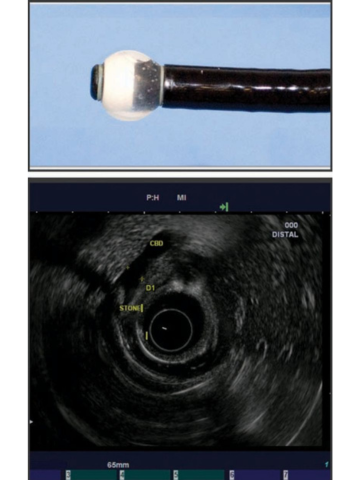
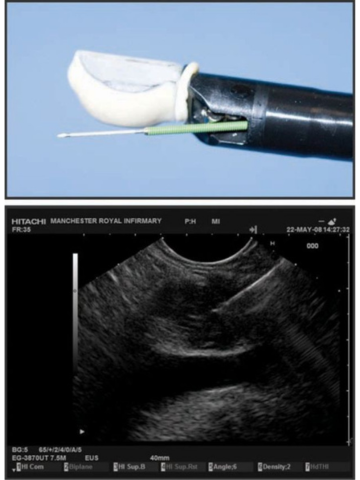
Існує два типи широко використовуваних ехоендоскопів, кожен з яких відрізняється своїми характеристиками. Радіальний ЕУЗД був першим, який був розроблений з забезпеченням 360-градусного огляду в площині, перпендикулярній до осцилографа, подібно до зображення комп’ютерної томографії (КТ) (мал. 2). Лінійне ехоендоскопічне ультразвукове дослідження забезпечує локалізоване косе зображення, паралельне ендоскопу, і дає змогу проводити терапевтичну діагностику ультразвуком (мал. 3). Також доступні високочастотні мінідатчики ЕУЗД, які можна пропускати через стандартний біопсійний канал ендоскопа у випадках, коли структури неможливо пройти за допомогою стандартного ендоскопа.
Показання до ендоскопічного УЗД
Показання до проведення ЕУЗД можна розділити на кілька категорій:
- визначення стадії злоякісних новоутворень ШКТ
- оцінка панкреатобіліарної хвороби
- оцінка субепітеліальних аномалій
- оцінка екстралюмінальних аномалій
- визначення стадії раку легенів
- терапевтичний ЕУЗД
Стадія раку шлунково-кишкового тракту
Точне визначення стадії злоякісної пухлини верхніх відділів шлунково-кишкового тракту є життєво важливим для вибору відповідного лікування для пацієнта. Завдяки своїй здатності розмежовувати різні шари стінки ШКТ, EUS тепер став невід’ємним компонентом у класифікації раку ШКТ за широко прийнятою класифікацією TNM.
Рак стравоходу
При раку стравоходу було доведено, що ЕУЗД є кращим за КТ сканування для точного визначення стадії. Також ЕУЗД є більш точним при оцінці лімфатичних вузлів черевної осі та зазвичай виконується, коли КТ не виявила віддалених метастазів. Це допомагає правильно відібрати пацієнтів для неоад’ювантної хіміопроменевої терапії. Пацієнти з дуже раннім раком стравоходу також можуть отримати користь від менш інвазивних процедур, таких як ендоскопічна резекція слизової оболонки. Мета аналіз, що порівнює КТ та ЕУЗД при раку стравоходу, показав, що точність визначення стадії (Т стадія) між двома методами становить 50–80% і 85–90%. Систематичний огляд ендоскопічного ультразвукового дослідження при раку шлунка та стравоходу, проведений NHS, підтверджує високу точність ЕУЗД для T і N стадії раку стравоходу.
Рак шлунка
Точність ЕУЗД у визначенні стадії раку шлунка не можна порівняти з раком стравоходу через складність диференціації підсерозного та серозного шарів. Проте багато досліджень продемонстрували перевагу ЕУЗД над звичайним КТ скануванням щодо точності визначення стадії, коливаючись від 71% до 88% (стадія T) і 77%-80% (стадія N). Обидва методи візуалізації є додатковими. УЗД є особливо корисним для визначення стадії раннього локалізованого раку шлунка для оцінки ендоскопічної резектабельності.
Рак підшлункової залози
Зображення високої роздільної здатності EUS для візуалізації протоки підшлункової залози та паренхіми роблять його високочутливим у виявленні невеликих пухлин, кіст та судинної інвазії. ЕНДО УЗД перевершує спіральну КТ, магнітно-резонансну томографію (МРТ) або позитронно-емісійну томографію (ПЕТ) у виявленні невеликих пухлин підшлункової залози з чутливістю визначення стадії понад 90%. Це також найбільш чутливий спосіб виявлення нейроендокринних пухлин підшлункової залози, що може розрізняти структури розміром до 2–3 мм.
Кістозні ураження підшлункової залози
Зі збільшенням доступності комп’ютерної томографії спостерігається постійне зростання кількості випадкових кістозних уражень підшлункової залози, і хоча більшість цих уражень невеликі та доброякісні, до 10% можуть являти собою злоякісні або передракові новоутворення. Попри прогрес у КТ та МРТ, здатність диференціювати доброякісні та злоякісні кісти залишається обмеженою. Ендоскопічна ультразвукова діагностика не тільки забезпечує зображення високої роздільної здатності, але також має додаткову перевагу взяття зразків вмісту кісти та будь-яких місцевих лімфатичних вузлів. ЕНДО УЗД FNA з цитологією при таких кістозних ураженнях може підвищити діагностичну точність.
Хронічний панкреатит
Ендоскопічне ультразвукове дослідження є дуже чутливим методом візуалізації для виявлення структурних змін хронічного панкреатиту, які можуть бути відсутніми при трансабдомінальному ультразвуковому дослідженні, КТ, МРТ або ендоскопічній ретроградній холангіопанкреатографії (ЕРХПГ). Однак слід бути обережним, тому що часто найскладнішою діагностичною інтерпретацією є вміння відрізнити хронічний очаговий панкреатит від гіпоехогенного утворення підшлункової залози у пацієнтів із хронічним панкреатитом. У цій ситуації позитивний EUS-FNA є дуже корисним, але низька чутливість при негативному EUS-FNA щодо злоякісності, означає що операція часто потрібна.
Холедохолітіаз
У пацієнтів із підозрою на жовчнокам’яну хворобу ЕУЗД має чутливість понад 90% у виявленні каменів в загальній жовчній протоці. Його можна порівняти з ЕРХПГ у діагностиці жовчнокам’яної хвороби, без властивих ризиків панкреатиту, але йому бракує терапевтичних можливостей для видалення каменів. Він значно перевершує трансабдомінальне ультразвукове дослідження, а контрольовані дослідження показали, що ЕУЗД порівняне або перевершує магнітно-резонансну холангіопанкреатографію у виявленні жовчнокам’яної хвороби.
Субепітеліальні ураження ШКТ
Ендоскопічне ультразвукове дослідження відіграє важливу роль в оцінці субепітеліальних уражень ШКТ. Цей метод може схарактеризувати ураження шляхом визначення їх розміру, країв, шару походження та текстури відлуння, а також може диференціювати екстрамуральні та інтрамуральні ураження. Найпоширенішими субепітеліальними ураженнями верхніх відділів шлунково-кишкового тракту є звичайні вдавлення на стінці, спричинені екстрамуральними органами, такими як печінка, селезінка, жовчний міхур або селезінкова вена. Доброякісні субепітеліальні ураження, ідентифіковані за допомогою EUS, включають ліпоми, прості кісти, вроджені кісти подвоєння, позаматкову тканину підшлункової залози та варикозне розширення вен. Злоякісні субепітеліальні ураження, діагностовані за допомогою ЕУЗД, включають метастази, лімфому та карциноїдні пухлини. Шлунково-кишкові стромальні пухлини (GISTS) все частіше розпізнаються, причому більшість цих уражень є доброякісними, але деякі мають злоякісний потенціал залежно від розміру, мітотичного індексу та локалізації. ЕУЗД-біопсія труката може дозволити диференціювати злоякісні та доброякісні GIST.
Лімфаденопатія середостіння
Ендоскопічне ультразвукове дослідження дозволяє легко ідентифікувати лімфатичні вузли в аортопульмональній, субкаринальній, паратрахеальній і параезофагеальній областях. EUS-FNA вузлів середостіння покращує діагностичну точність у визначенні злоякісної ознаки, отже, дозволяє уникнути медіастиноскопії чи торакотомії. Показано, що ЕУЗД FNA дає змогу встановити діагноз, якщо результати КТ, ПЕТ, бронхоскопії та плевроцентезу були негативними або безрезультатними. Чутливість ЕУЗД FNA для виявлення злоякісних новоутворень у лімфатичних вузлах середостіння становить 88–96%15, а також можна диференціювати туберкульоз, саркоїдоз та лімфому та трукат-біопсії без необхідності інвазивної медіастиноскопії. Нещодавня розробка тканинної еластографії для визначення злоякісного потенціалу лімфатичних вузлів шляхом аналізу щільності тканини лімфатичних вузлів також можлива за допомогою ЕНДО УЗД, що може допомогти уточнити ЕУЗД-FNA підозрілого вузла.
Ендоскопічне УЗД у визначенні стадії раку легенів
Визначення стадії раку легенів залежить від трансбронхіальної біопсії, FNA під контролем КТ, медіастиноскопії з біопсією або торакоскопії. Доведено, що EUS-FNA є точною та безпечною процедурою визначення стадії лімфатичних вузлів у пацієнтів із задокументованим раком легенів. EUS-FNA також має здатність ідентифікувати вузли середостіння, пропущені під час КТ, а також при не дрібноклітинному раку легенів. ЕУЗД виявилося точним і економічно ефективним для визначення стадії вузлів у пацієнтів із підтвердженою лімфаденопатією заднього середостіння з чутливістю 83% і специфічністю 97%. Нещодавно було показано, що ендобронхіальне ультразвукове дослідження (EBUS) доповнює EUS, що дозволяє майже повне мінімальне інвазивне медіастинальне визначення стадії у пацієнтів з підозрою на рак легенів з діагностичною точністю 90–100%.
Терапевтичне ендоскопічне УЗД
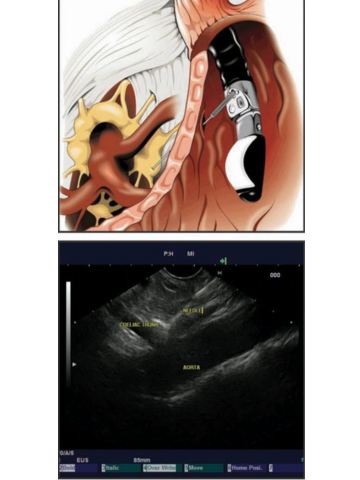
Початкова розробка EUS-FNA прогресувала, щоб забезпечити нові та нові терапевтичні показання для ЕНДО УЗД. Блокування целіакічного сплетення та нейроліз за допомогою ін’єкції стероїдів або спирту під контролем EUS у черевне сплетення, а останнім часом безпосередньо в ганглії целіакії, є безпечним та ефективним методом контролю болю при раку підшлункової залози та, меншою мірою, при хронічному панкреатиті (мал. 4).
Дренування симптоматичних псевдокіст раніше проводилося наосліп за допомогою прямого ендоскопічного доступу або необхідного хірургічного втручання. ЕУЗ цистогастростомія дозволяє охарактеризувати псевдокісту, провести пряму пункцію в кісту під візуалізацією ЕУЗД (уникаючи будь-яких судин) і встановити стент за одну процедуру, причому перебування пацієнта коротше, ніж хірургічне втручання. Це має бути лікуванням вибору для симптоматичних неускладнених псевдокіст, якщо це можливо. ЕУЗД також можна використовувати для доступу до жовчовивідної системи, коли ERCP не вдається шляхом пункції загальної жовчної протоки дротом під контролем EUS і може виявити та дренувати асцит.
Експериментальне застосування EUS, яке зараз вивчається, включає місцеве проведення брахітерапії або хіміотерапії при поширеному раку підшлункової залози, алкогольну абляцію метастазів у надниркових залозах або нейроендокринних пухлин підшлункової залози та імплантацію рентгеноконтрастних маркерів під слизову оболонку під контролем ЕНДО УЗД перед променевою терапією. Швидкий розвиток ендоскопічної транслюмінальної хірургії через природні отвори стрирає межі між ендоскопією та хірургією, а ЕУЗД відіграє ключову роль у її майбутньому.
Це безпечна та економічно ефективна процедура, яка має значний вплив на лікування пацієнтів із раком стравоходу та стравохідно-шлункового з’єднання з метою точного визначення стадії захворювання. Це також найбільш чутливий метод виявлення злоякісних новоутворень підшлункової залози для визначення природи субепітеліальних уражень і відіграє додаткову роль у визначенні стадії недрібноклітинного раку легені. Його терапевтичний потенціал продовжує зростати, оскільки з’являються нові показання та процедура поступово стає доступнішою.
Матеріали для публікації використатні з сайту https://www.ncbi.nlm.nih.gov
Посилання: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4952290/
